|
||||||||||||
|
||||||||||||
|
||||||||||||
| 国立感染症研究所感染症疫学センター 病原微生物検出情報事務局 |
|
||||||||||||
|
||||||||||||
|
||||||||||||
| 国立感染症研究所感染症疫学センター 病原微生物検出情報事務局 |
| 国立感染症研究所・感染症情報センターには地方衛生研究所(地研)から「病原体個票」が報告されている。これには感染症発生動向調査の定点およびその他の医療機関、保健所等で採取された検体から検出された病原体の情報が含まれる(参考図)。 |
|
|||||
|
*2014/15シーズンは2014年第36週/9月~2015年第35週/8月(検体採取週)。 図の元データは、以下の速報グラフ(病原体個票による報告)。 データは、土日祝日を除く2日前に地研から報告された情報。過去の週に遡っての追加報告もある。現在報告数は、地研より報告された日を表す。 |
| 国立感染症研究所感染症疫学センター 病原微生物検出情報事務局 |
 |
国立感染症研究所インフルエンザウイルス研究センター第一室
全国地方衛生研究所 |
| 国立感染症研究所・感染症情報センターには地方衛生研究所(地研)から「病原体個票」が報告されている。これには感染症発生動向調査の定点およびその他の医療機関、保健所等で採取された検体から検出された病原体の情報が含まれる(参考図)。 |
|
||||||
|
*2014/15シーズンは2014年第36週/9月~2015年第35週/8月(検体採取週)。 図の元データは、以下の速報グラフ(病原体個票による報告)。 データは、土日祝日を除く2日前に地研から報告された情報。過去の週に遡っての追加報告もある。現在報告数は、地研より報告された日を表す。
|
| 国立感染症研究所感染症疫学センター 病原微生物検出情報事務局 |
|
||||||||||||
|
||||||||||||
|
||||||||||||
| 国立感染症研究所感染症疫学センター 病原微生物検出情報事務局 |
SFTSは2011年に中国の研究者らによって発表されたブニヤウイルス科フレボウイルス属に分類される新しいウイルスによるダニ媒介性感染症である。2013年1月に国内で海外渡航歴のない方がSFTSに罹患していたことが初めて報告され、それ以降他にもSFTS患者が確認されるようになった。SFTSウイルス(SFTSV)に感染すると6日〜2週間の潜伏期を経て、発熱、消化器症状(食欲低下、嘔気、嘔吐、下痢、腹痛)が多くの症例で認められ、その他頭痛、筋肉痛、意識障害や失語などの神経症状、リンパ節腫脹、皮下出血や下血などの出血症状などを起こす。検査所見上は白血球減少、血小 板減少、AST・ALT・LDHの血清逸脱酵素の上昇が多くの症例で認められ、血清フェリチンの上昇や骨髄での血球貪食像も認められることがある。致死率は6.3〜30%と報告されている。感染経路はマダニ(フタトゲチマダニなど)を介したものが中心だが、血液等の患者体液との接触により人から人への感染も報告されている。治療は対症的な方法しかなく、有効な薬剤やワクチンはない。
 フタトゲチマダニ Haemaphysalis longicornis
フタトゲチマダニ Haemaphysalis longicornis
感染症発生動向調査では110人のSFTS患者が報告されており、男女比は24:31で、年齢中央値は73歳であった。 5-8月の発症例が多く、西日本の15県から報告されている。なお、感染症発生動向調査で届出が求められる以前に診断された4人の患者は報告されていない。
表1 基本情報(2015年3月11日現在)
| 生存例 | 死亡例 | 合計 | ||
| 報告数 | 78 | 32 | 110 | |
| 性別 | 男 | 35 | 13 | 48 |
| 女 | 43 | 19 | 62 | |
| 年齢 | 中央値 |
70.5歳 |
80.5歳 |
73歳 |
| ~20代 | 1 | 0 | 1 | |
| 30代 | 1 | 0 | 1 | |
| 40代 | 2 | 0 | 2 | |
| 50代 | 5 | 2 | 7 | |
| 60代 | 27 | 5 | 32 | |
| 70代 | 21 | 8 | 29 | |
| 80代 | 18 | 14 | 32 | |
| 90代~ | 3 | 3 | 6 |
注)死亡は感染症発生動向調査の届出時点の情報であり、経過中の死亡は報告されていない可能性がある
図1 2013年1月1日以降に発症したSFTS症例の発症時期(N=102, 2015年3月11日現在)
図2 SFTS症例の発生(感染)地域(N=110, 2015年3月11日現在)
(国立感染症研究所 ウイルス第一部・感染症疫学センター)
| 2014年02月25日 | <速報>重症熱性血小板減少症候群(SFTS)ウイルスの国内分布調査結果(第二報) |
| 2014年2月 | <特集>日本における重症熱性血小板減少症候群 |
| 2014年2月 | 上記特集関連情報 |
| 2013年10月25日 | 家族内発症2名の重症熱性血小板減少症候群(SFTS)患者を含むSFTS患者5名の臨床的特徴 |
| 2013年09月24日 | 山口県の一医療機関における重症熱性血小板減少症候群症例の接触者調査 |
| 2013年08月29日 | <速報>重症熱性血小板減少症候群(SFTS)ウイルスの国内分布調査結果(第一報) |
| 2013年07月23日 | フタトゲチマダニ刺咬後に早期診断され良好な経過をたどった重症熱性血小板減少症候群の1例 |
| 2013年03月14日 | 国内で確認された重症熱性血小板減少症候群(SFTS)患者8名の概要(2013年3月13日現在) |
| 2013年03月07日 | 国内で初めて確認された重症熱性血小板減少症候群(SFTS)患者に続いて後方視的に確認された2例 |
| 2013年01月30日 | 国内で初めて診断された重症熱性血小板減少症候群患者 |
| 2013年02月19日 | 重症熱性血小板減少症候群(SFTS)の国内での確認状況について(情報提供)(その2) (PDF) |
| 2013年02月13日 | 重症熱性血小板減少症候群(SFTS)の国内での確認状況について(情報提供) (PDF) |
| 2013年01月30日 | 重症熱性血小板減少症候群(SFTS)について [結核感染症課長通知] (PDF) |
| 2013年01月30日 | 重症熱性血小板減少症候群について(PDF) |
| 2013年01月30日 | 重症熱性血小板減少症候群に関するQ&A(PDF) |
図1.月別麻疹ウイルス分離・検出報告数、2010~2015年 CSV
図2.麻疹ウイルス分離・検出例の年齢分布、2012~2015年
図3.遺伝子型別都道府県別麻疹ウイルス分離・検出報告状況、2012~2015年
2015年 PDF CSV (2015年2月24日現在報告数)
2014年 PDF CSV (2015年2月24日現在報告数)
2013年 PDF CSV (2015年1月20日現在報告数)
|
|
 |
国立感染症研究所インフルエンザウイルス研究センター第一室
全国地方衛生研究所 |
|
日本は世界最大の抗インフルエンザ薬使用国であり、薬剤耐性株の検出状況を迅速に把握し、自治体および医療機関に情報提供することは公衆衛生上重要である。そこで全国地方衛生研究所(地研)と国立感染症研究所(感染研)では、オセルタミビル(商品名タミフル)、ザナミビル(商品名リレンザ)、ペラミビル(商品名ラピアクタ)およびラニナミビル(商品名イナビル)に対する薬剤耐性株サーベイランスを実施している。 下記のグラフおよび表に、地研が遺伝子解析により耐性マーカーH275Yを検出した結果および感染研においてオセルタミビル、ザナミビル、ペラミビルおよびラニナミビルに対する薬剤感受性試験を行った結果の集計を示す。集計結果は随時更新される。 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2015年03月17日 | デング熱の流行状況について (更新2) |  |
| 2015年02月25日 | ブルネイ でデング熱が流行しています | |
| 2015年02月24日 | ブラジル・サンパウロ州でデング熱が流行しています | |
| 2015年02月18日 | デング熱の流行状況について (更新1) | |
| 2015年01月22日 | デング熱の流行状況について |
 |
国立感染症研究所インフルエンザウイルス研究センター第一室
全国地方衛生研究所 |
|
日本は世界最大の抗インフルエンザ薬使用国であり、薬剤耐性株の検出状況を迅速に把握し、自治体および医療機関に情報提供することは公衆衛生上重要である。そこで全国地方衛生研究所(地研)と国立感染症研究所(感染研)では、オセルタミビル(商品名タミフル)、ザナミビル(商品名リレンザ)、ペラミビル(商品名ラピアクタ)およびラニナミビル(商品名イナビル)に対する薬剤耐性株サーベイランスを実施している。 下記のグラフおよび表に、地研が遺伝子解析により耐性マーカーH275Yを検出した結果および感染研においてオセルタミビル、ザナミビル、ペラミビルおよびラニナミビルに対する薬剤感受性試験を行った結果の集計を示す。集計結果は随時更新される。 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
(2014年12月21日~2015年2月20日受理分)
|
| 国立感染症研究所細菌第一部第二室 |

(IASR Vol. 36 p. 136: 2015年3月号)
デングウイルスは、フラビウイルス科に分類され、1~4型の4つの血清型がある。デングウイルスは、ネッタイシマカ(Aedes aegypti)やヒトスジシマカ(Aedes albopictus)の刺咬により人→蚊→人→蚊の感染環において自然界に存在する。ネッタイシカは都市部に多く生息し、ヒトスジシマカは都市部と郊外の両方に生息する。日本では、ヒトスジシマカは国内の広範な地域生息している。人は感染蚊の刺咬後、通常3~7日程度の潜伏期を経て発熱、発疹、疼痛(関節痛)を3主徴とするデング熱を発症する(本号3、6&9ページ; IASR 35: 241-242, 2014)。デング熱は熱帯・亜熱帯地域で流している(本号14ページ)。特異的な治療法や実用化されたワクチンはなく(本号12ページ)、輸液や解熱鎮痛薬などで対処する。稀に一部のデング熱患者が、出血、ショック症状を呈し、死に至る危険性もある。適切な治療により致命率を減少させることができる。
感染症発生動向調査:感染症法に基づく感染症発生動向調査では、デング熱は全数把握の4類感染症として診断後直ちに届け出ることが医師に義務付けられている(デング熱・デング出血熱の届出基準はhttp://www.mhlw.go.jp/bunya/kenkou/kekkaku-kansenshou11/01-04-19.html参照)。
デング熱(デング出血熱を含む)の報告数は、2007~2009年には年間89~105例であったが、2010年、2012年と2013年は200例以上であった(図1、表1)(2004~2010年の状況はIASR 32: 159-160,2011参照)。2014年には約70年ぶりに162例の国内感染例が報告され(本号3、5&6ページ)、国外感染例(以下輸入例)の179例を含めると計341例が報告された(表1およびhttp://www.nih.go.jp/niid/ja/dengue-m/dengue-iasrs/5410-pr4211.html参照)。近年デングウイルス1型が最も多く検出されている(表2)。2014年に国内で流行した血清型も1型であった(本号3, 5, 6&8ページ)。
患者発生の季節性:例年8~9月に患者の増加が認められる(IASR 32: 159-160, 2011参照 )(図1)。このことは、渡航先のその時期におけるデング熱の流行状況と旅行者数の二つの因子が影響していると考えられる。2014年の国内感染例も162例中133例(82%)が9月に診断されている(図1)。
推定感染地:2011~2014年に診断された輸入例の渡航先は、少なくとも37カ国/地域であった(表3)。2011~2013年に報告された輸入例583例のうち554例(95%)の渡航先は、アジア地域、特に東南アジアであった。例年、インドネシア、フィリピン、タイ、インド、カンボジア、マレーシアなどへ渡航して感染した輸入例が多く、これは渡航先でのデング熱流行状況(本号14ページ)と日本からの渡航者数の多さを反映していると思われる。その他に、中南米、オセアニア、アフリカで感染したと推定された輸入例も報告された。2014年の輸入例179例中165例(92%)の推定感染地はアジア地域であった。2014年に日本で発生したデング熱流行では162例の国内感染例が報告されたが、159例(98%)の推定感染地は東京都であった(本号3&5ページ参照)。
性別と年齢:2011~2014年に報告された輸入例762例の性別は、男471例(62%)、女291例(38%)であり、年齢は20代が218例(29%)、30代201例(26%)、40代126例(17%)であった(図2)。2014年の国内感染例の性別も、162例中95例(59%)が男性であり、男性患者が多かった。国内感染例の年齢は4~77歳(中央値27歳)であり、幅広い年齢層で国内感染が認められた(図2)。
デング出血熱:近年、報告されている輸入例(デング熱・デング出血熱症例)の約5%がデング出血熱を発症していた〔2011年4/113 (4%)、2012年13/221 (6%)、2013年11/249 (4%)、2014年8/179(4%)〕(表1)。2011~2014年に報告されたデング出血熱症例37例の年齢は3~64歳(中央値32歳)で、この期間に報告された全輸入例(デング熱・デング出血熱症例)に占めるデング出血熱の割合には、男女差はなかった〔男23/471 (5%)、女13/291(4%)〕。2014年の国内流行では、162例の国内感染例のうち、デング出血熱を発症した患者は1例(1%)であった。2011~2014年においては死亡例の報告はなかった。
実験室診断:ウイルス分離検査、RT-PCRによる遺伝子検査、血清学的検査(IgM抗体検出、中和抗体検出など)のデング熱実験室診断は、地方衛生研究所(地衛研)、国立感染症研究所において実施可能である(本号8ページ)。検疫法の改正により2003年11月にデング熱が検疫感染症に加えられ、検疫所では流行地域からの入国者を対象に健康相談および必要に応じて検査がなされている(IASR 35: 112-114, 2014)。2013年4月に感染症発生動向調査の届出基準におけるデング熱診断方法に非構造タンパクNS1抗原検出法が追加され(平成25年3月7日健感発0307第2号厚生労働省健康局結核感染症課長通知)、その迅速診断検査キットが2014年のデング熱国内流行時に地衛研等に配布された(本号8&9ページ)。2013年以降では、RT-PCRによる遺伝子検出、IgM抗体検出、非構造タンパクNS1抗原検出により実験室診断される例が大半である(表4)。
わが国での対策:デングウイルス媒介蚊のひとつであるヒトスジシマカが日本国内に生息すること(本号10ページ)、また、海外の流行地で感染した者が入国する例が増加傾向にあることから、国内で蚊と人の間で感染環が成立し、これからも国内でデング熱が発生・流行する可能性がある。2014年の国内流行時には日本でデングウイルスに感染し、帰国先でデング熱を発症したいわゆる輸出例も報告されている(本号7ページ)。国際化が進み人の移動が盛んになっていることから、デング熱流行の予防と対策は非流行国である日本においても重要である。
蚊媒介感染症のまん延防止等のために、厚生労働省は「蚊媒介感染症に関する特定感染症予防指針」を2015年4月中に告示する予定である。本指針においては、デング熱とチクングニア熱(本号15&16ページ)対策の重要な軸として、平時から感染症を媒介する蚊の対策を行うこと、国内において蚊媒介感染症例の発生を迅速に把握すること、発生時に的確な媒介蚊の対策を行うこと、患者に適切な医療を提供することが挙げられている。デング熱の発生・流行の対策には、医療関係者、行政関係者、国民が協力してその予防に取り組んでいくことが求められる。
|
||||||||||||
|
||||||||||||
|
||||||||||||
| 国立感染症研究所感染症疫学センター 病原微生物検出情報事務局 |
| 国立感染症研究所・感染症情報センターには地方衛生研究所(地研)から「病原体個票」が報告されている。これには感染症発生動向調査の定点およびその他の医療機関、保健所等で採取された検体から検出された病原体の情報が含まれる(参考図)。 |
|
||||||
|
*2014/15シーズンは2014年第36週/9月~2015年第35週/8月(検体採取週)。 図の元データは、以下の速報グラフ(病原体個票による報告)。 データは、土日祝日を除く2日前に地研から報告された情報。過去の週に遡っての追加報告もある。現在報告数は、地研より報告された日を表す。
|
| 国立感染症研究所感染症疫学センター 病原微生物検出情報事務局 |
 |
国立感染症研究所インフルエンザウイルス研究センター第一室
全国地方衛生研究所 |
|
日本は世界最大の抗インフルエンザ薬使用国であり、薬剤耐性株の検出状況を迅速に把握し、自治体および医療機関に情報提供することは公衆衛生上重要である。そこで全国地方衛生研究所(地研)と国立感染症研究所(感染研)では、オセルタミビル(商品名タミフル)、ザナミビル(商品名リレンザ)、ペラミビル(商品名ラピアクタ)およびラニナミビル(商品名イナビル)に対する薬剤耐性株サーベイランスを実施している。 下記のグラフおよび表に、地研が遺伝子解析により耐性マーカーH275Yを検出した結果および感染研においてオセルタミビル、ザナミビル、ペラミビルおよびラニナミビルに対する薬剤感受性試験を行った結果の集計を示す。集計結果は随時更新される。 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
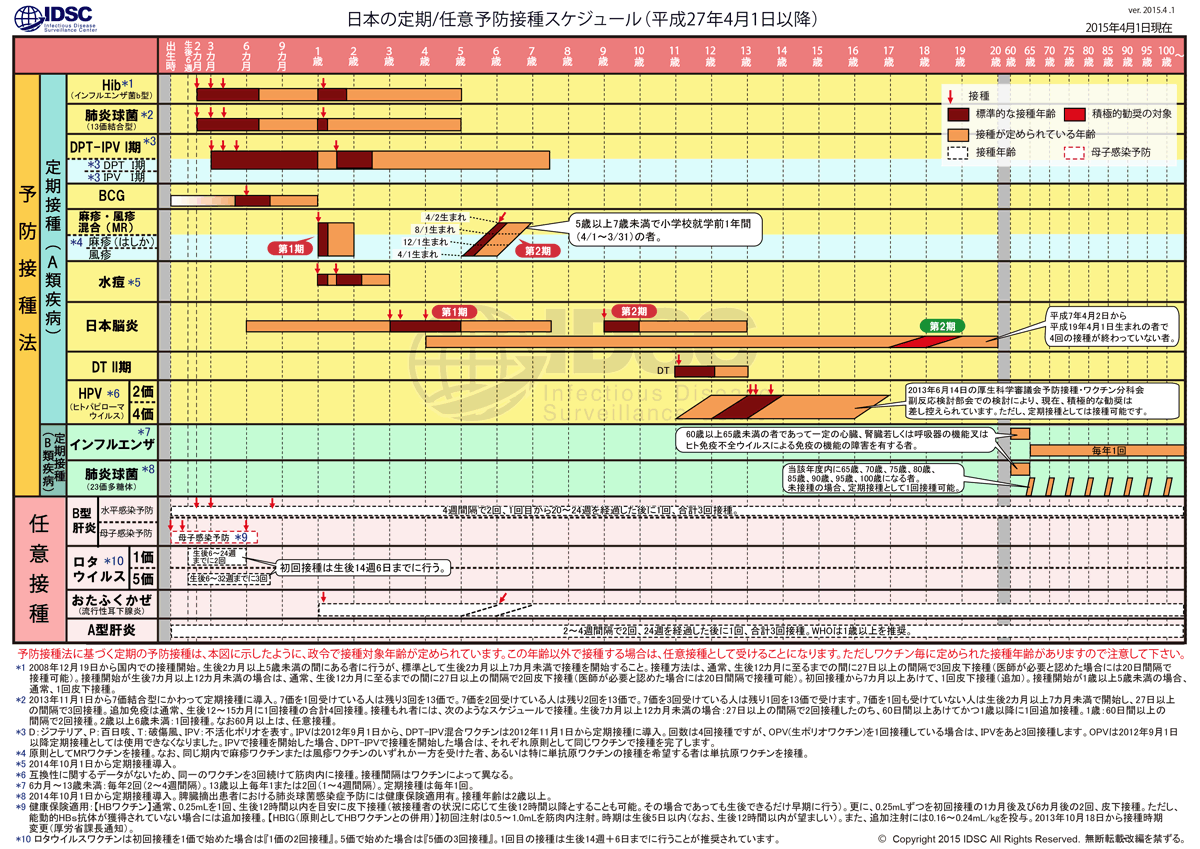
(日本の予防接種スケジュール) |
| (2015年4月1日更新) |
| 〔2015年4月1日~〕 | 全年齢 | ||
 |
日本語(2015年4月1日~) | ||
| ○ 画面で見る(GIF)-NEW ○ PDFをダウンロード |
|||
| English (applicable after April 1, 2015) | |||
| ○ See image(GIF) ○ Download PDF |
|||
| → 過去のスケジュール一覧はこちらからご覧になれます。 |
 |
 |
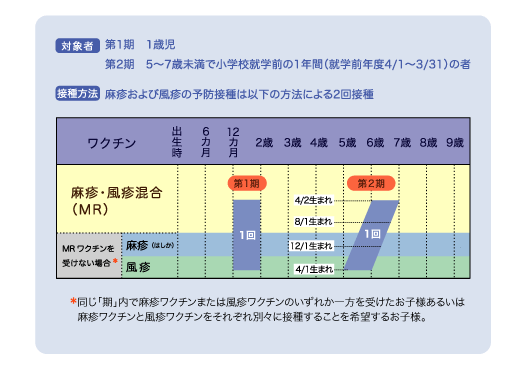
2006年4月1日以降、定期の予防接種としては麻疹・風疹混合生ワクチン (measles-rubella:MRワクチン)の接種が開始となり、 同年6月2日から下記の年齢での2回接種となりました。 第1期、第2期を過ぎてしまうと定期の予防接種として受けられなくなってしまいます。 小学校の入学前に接種がすんでいるかどうかを確認しましょう。 第2期でまだ麻疹と風疹の予防接種をそれぞれ2回ずつ受けていないお子さまは、 かかりつけ医とよく相談し、2016年3月31日までに受けましょう。 |
 接種医療機関に関しては、お住まいの市町村(特別区)にお尋ねください。 接種医療機関に関しては、お住まいの市町村(特別区)にお尋ねください。 |
(IDSC更新 2015/4/1 )
(掲載日 2015/4/1)
手足口病は通常、夏季に流行し、Enterovirus A 71(EV-A71)、Coxsackievirus A6(CV-A6) およびCV-A16が主な原因ウイルスとして知られている。大阪府では、ピーク時の定点あたりの患者数が8.03であった2013年度と比較して0.51であった2014年度は、手足口病の流行が非常に低調であったが、例年とは異なり、冬季にも患者数の増加が認められた。また、患者から検出されたウイルスの種類にも特徴が認められた。本稿では大阪府における2014年度の手足口病疑い患者の発生動向と検出されたウイルスの遺伝子型の特徴を報告する。
感染症発生動向調査事業に基づき指定の医療機関(病原体定点)から大阪府立公衆衛生研究所に搬入された手足口病疑い患者検体を対象に、咽頭ぬぐい液、唾液および糞便検体からウイルスRNAを抽出し、エンテロウイルスVP4-2領域を標的としたRT-semi-nested PCR1)を実施した。増幅産物をダイレクトシークエンスした結果を用いてウイルスの遺伝子型別を行った。さらに、すべての検体に対し、Human parechovirus(HPeV)に対するRT-real time PCR2)を実施した。
2014年4月1日~2015年3月6日までの期間に、手足口病疑い患者検体は計47検体搬入され、そのうち37検体からウイルス遺伝子が検出された。重複感染で検出されたものを含めたウイルスの検出頻度は多い順にCV-A16(17検体)、HPeV(10検体)、Rhinovirus(RV、6検体、CV-A6(4検体)、EV-A71、CV-A2、CV-A4、CV-A5、CV-A10(各1検体)であった。HPeVが検出された10検体のうち4検体が重複感染で、重複していたウイルスはそれぞれCV-A4、RV、CV-A16、RVとCV-A6であった。CV-A16が検出されたのは2014年第35週~2015年第9週、HPeVが検出されたのは 2014年第25~32週であった(図1)。臨床的には2014年夏季のHPeVが単独で検出された手足口病患者では手足の水疱が不鮮明であるとの報告が散見されたが、冬季のCV-A16が検出された患者では典型的な症状を呈する手足口病との報告が多数であった。なお、手足口病患者からHPeVが検出されていた時期のヘルパンギーナ患者検体74検体中10検体(14%)からもHPeVが検出されていた。
大阪府の手足口病患者数の推移を全国と比較すると、全国的にも低流行ではあったが、例年どおり夏季に症例数が多く冬季は低レベルで推移しているのに対し(図2)、大阪府では夏季と冬季に同程度の患者数の増加を示している点で特徴的であった。NESIDから得た情報によると、2014年の夏季における全国の手足口病患者からのウイルス検出はEV-A71およびCV-A16が主で、冬季にはCV-A16が主となった。大阪府における手足口病は、2014年の夏季にHPeVが、冬季にCV-A16が主な流行の原因だった点でも全国の発生動向とは異なる傾向を示した。
2014年度大阪府で認められた夏季と冬季の二峰性の患者数の推移は、手足口病の典型的な季節的流行パターンとは異なっていた。また、病原体も通常みられるウイルスとは異なり、夏季の症例でHPeV陽性例が目立った。HPeVは通常手足口病の原因になるウイルスとは考えられていないため、感染症発生動向調査事業では検出を行っていない場合もある。しかし、HPeV感染による発疹は臨床的には通常の手足口病と明確には区別しにくいため、手足口病の起因ウイルスの検索にはHPeVを含めた病原体検出を念頭に置く必要があると考えられる。